Anvisa suspende lote de camomila da marca Água da Serra que apresentou 224 fragmentos e 14 larvas de insetos em amostra; produto para cuidados com tatuagem também é proibido por falta de registro. Cateter intravenoso da Injex sofre suspensão por defeito.
A Agência Nacional de Vigilância Sanitária (Anvisa) emitiu alerta com medidas de recolhimento e suspensão de produtos considerados irregulares, que vão desde um chá de camomila contaminado até uma pomada para tatuagem sem registro. As decisões foram publicadas no Diário Oficial da União (DOU) e evidenciam falhas que podem colocar a saúde do consumidor em risco.

Chá de Camomila com contaminação por insetos
O caso mais grave é o do Chá de Camomila Lavi Tea, da marca Água da Serra, lote 6802956. A empresa Água da Serra Industrial de Bebidas S.A. comunicou um recolhimento voluntário do produto, o que foi seguido por uma determinação formal da Anvisa. A agência suspendeu a comercialização, distribuição, propaganda e uso do lote.
Os motivos são graves: laudos técnicos apontaram dois problemas principais: identificação de elementos histológicos: presença de talos, ramos e sementes que não são comuns ou típicos na composição do chá de camomila; presença de matérias estranhas: a análise encontrou uma contaminação por insetos muito acima do limite tolerado. Em uma amostra de 25 gramas do produto, foram identificados 224 fragmentos de insetos e 14 larvas inteiras. O limite máximo aceitável pela legislação é de 90 fragmentos na mesma quantidade de produto.

Pomada para tatuagem é proibida por falta de registro
Outro produto alvo da fiscalização é a Pomada Cicatrizante Inkdraw Aftercare, indicada para uso pós-tatuagem. A Anvisa determinou a proibição total da comercialização, distribuição, fabricação, importação, propaganda e uso do item.
O motivo é a falta de regularização sanitária: a pomada não possui registro ou notificação junto à Anvisa e é de origem desconhecida, pois a empresa responsável não está identificada na base da agência. A venda era feita pelo site inkdraw.com.br.
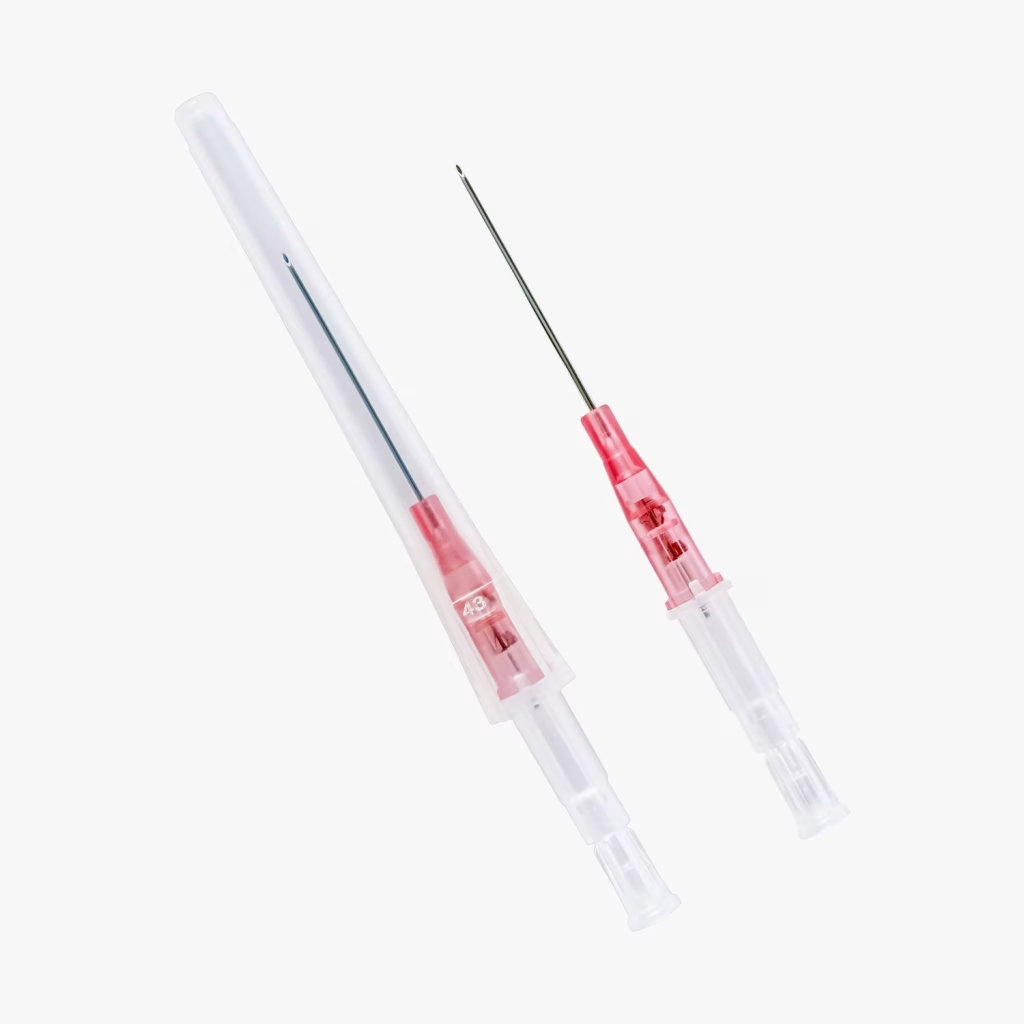
Cateter intravenoso suspenso por defeito
Além dos casos publicados nesta segunda, a fiscalização da Anvisa também resultou, ainda em dezembro de 2025, na suspensão de um dispositivo médico. Trata-se do Cateter Intravenoso com Dispositivo de Segurança Injex-Cath® SAFETY, lote 22300/095, fabricado pela INJEX Indústrias Cirúrgicas Ltda.
A medida, que inclui recolhimento e proibição de comercialização, distribuição, propaganda e uso, foi tomada após análise fiscal da Fundação Ezequiel Dias (FUNED). O laudo apontou resultado insatisfatório no teste de acabamento da superfície e aparência visual da agulha, que apresentou um defeito na superfície externa do tubo. O produto estava em desacordo com a norma técnica ABNT NBR ISO 9626:2020.










Você precisa fazer login para comentar.